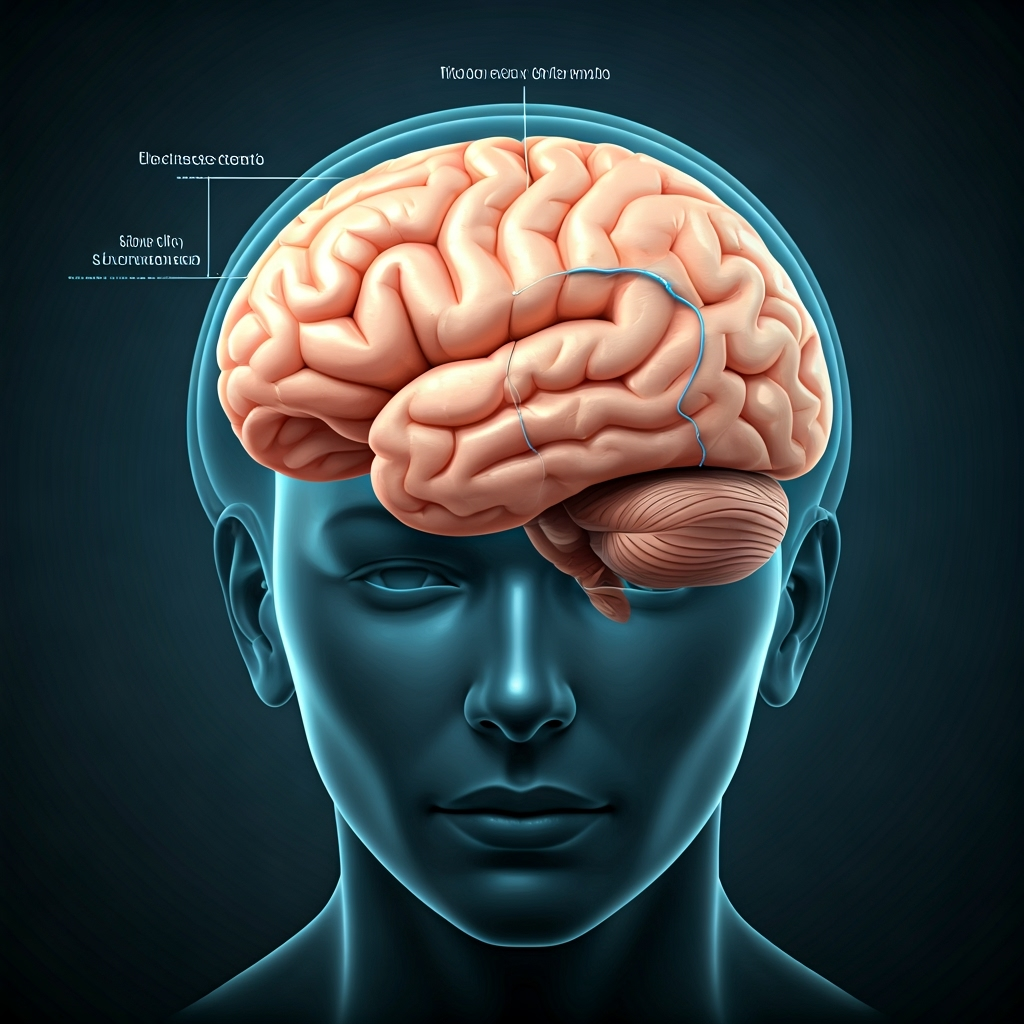
Elon Musks Neurotechnologie-Unternehmen Neuralink hat die behördliche Genehmigung erhalten, seine Gehirn-Computer-Schnittstelle (BCI) einem zweiten Patienten zu implantieren. Die Freigabe durch die US-amerikanische Food and Drug Administration (FDA) erfolgte, nachdem das Unternehmen erhebliche Modifikationen an seinem Gerät vorgenommen hatte, um ein mechanisches Problem zu beheben, das während der ersten wegweisenden Studie festgestellt wurde.
Der erste Patient, der 29-jährige Noland Arbaugh, der von den Schultern abwärts gelähmt ist, konnte erfolgreich einen Computercursor mit seinen Gedanken steuern. Einige Wochen nach der Operation im Januar begannen sich jedoch einige der ultrafeinen Fäden des Implantats aus seinem Hirngewebe zurückzuziehen. Dies führte zu einer Verringerung der Anzahl aktiver Elektroden und einer verminderten Datenerfassungsleistung des Geräts. Zwar konnten die Ingenieure von Neuralink die Leistung wiederherstellen, indem sie ihre Algorithmen so verfeinerten, dass sie empfindlicher auf die verbleibenden Elektrodensignale reagierten, doch das Hardwareproblem erforderte eine direkte Lösung für zukünftige Patienten.
Um ein erneutes Auftreten dieses Problems zu verhindern, wird Neuralink die Fäden des Implantats nun tiefer in den motorischen Kortex des Gehirns einbetten. Das Unternehmen plant, die Fäden acht Millimeter tief einzubringen – eine deutliche Steigerung gegenüber den drei bis fünf Millimetern beim ersten Eingriff. Diese strategische Anpassung soll für mehr Stabilität sorgen und sicherstellen, dass die Fäden sicher an ihrem Platz bleiben.
Diese Entwicklung unterstreicht den iterativen und anspruchsvollen Charakter der Entwicklung modernster Medizintechnik. Neuralinks Fähigkeit, das Problem zu identifizieren, eine Lösung zu entwickeln und die rasche behördliche Genehmigung für die Modifikation zu erhalten, ist ein entscheidender Schritt vorwärts in seiner Mission, Menschen mit Lähmungen zu helfen. Das Unternehmen plant, das Gerät noch in diesem Jahr dem zweiten Patienten zu implantieren und strebt bis Ende 2024 insgesamt zehn Implantationen beim Menschen an, vorbehaltlich weiterer FDA-Zulassungen. Der Erfolg dieser nächsten Eingriffe wird entscheidend für die langfristige Lebensfähigkeit und Sicherheit der Technologie sein.